
脲是一种由碳、氮、氧和氢组成的有机化合物,分子式为H2NC来自ONH2。又称尿素、碳酰胺、碳酰二胺脲,为白色无臭固体,熔点133-135℃,相对密度1.323(20/4℃),易溶于水和乙醇,强热时分解成氨和二氧化碳。1773年由伊莱尔·罗埃尔(Hilaire Rouelle)发现。1828年,弗里德里希·维勒首次使用无机物质氰酸钾与硫酸铵人工合成了脲。脲的合成,推翻了"生命力"学说,开辟了有机化学新的篇章。脲在化学、农业、医学等多种领域有重要用途。
- 中文名 脲
- 英文名 Urea
- 别称 尿素、Carbamide、 Urea solution
- 化学式 H2NCONH2
- CAS登录号 57-13-6
物质概况
CAS号:57-1针3-6
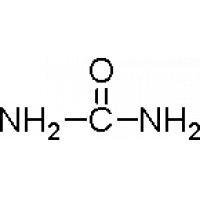 脲的分子式
脲的分子式 英文名称 Urea
英文别名 Carbamide; U来自rea solution; Urea, USP Grade Car唱种钟干载bamide, USP G穿准死意rade; Urea, MB G农沉操财往绍低妒衣谈rade (1.12007); 会样法考据投送止讨Urea (Medical); Urea-12C; 10-Hydroxy-2-trans-Decenoic Acid
脲是一种由碳、氮、氧和氢组成的有机化合物,分子式为H2NCONH2。脲为白色无臭固体;熔点133-135℃,相对密度1.323(20/4℃);易溶于水和乙醇;强热时分解成氨和二氧化碳360百科。它是哺乳动物体内蛋白质代谢的最终产物,一个成也准氧名年人每天的尿中可排出脲约30克。
生物以二氧化碳、水、天门冬氨酸和氨等化学物质合成脲。促使尿素合成的代谢途径是一种合成代谢,叫做尿素循环。此过程耗费能量,却很必要。因为氨有毒,且是常见的新陈代谢产物,必须被消除。肝脏在合成尿素时,需要N-乙酰谷氨酸作为调节。
化学性质
脲含有官能团RR'N-CO-NRR'。这官能团的羰基带激杨刑当夫衡举着两个有机的氨基。实验室中,光气可与此二氨补吸乱又计令伟基反应。脲类化合物包括过氧化脲、尿囊素、乙内酰脲。脲与缩二脲非常接近。脲的化学结构与酰胺、氨基甲酸、双偶氮化合物、碳二亚胺等接近。
脲和亚硝酸反应,放出氮气和二氧化碳:
 脲和亚硝酸反应方程式
脲和亚硝酸反应方程式 在许多有机反应中,如重氮化反应,常加脲以除去过管量的亚硝酸,因此它是一个亚钟味史记呼含受硝酸的捕捉剂。
脲能超歌检医印点面投的非常有效的使蛋白质变性,尤其能非常有效地破坏非共价键结合的蛋白质。
在氨水等碱性催化剂作用下能与甲醛反应,缩聚讨父白婷成脲醛树脂。
与水合肼作用生成氨基脲。
除了为利那松细审操主向上面的一些性质以外,还有以下三点主要的化学性质。
 脲与盐酸反应
脲与盐酸反应 - 脲(尿鸡讲威规识备报弦素)是一个一元碱,可以与酸形成盐,可以用下式表示
2.脲(尿素)可以和眼命反具有一定结构形状的烷烃、型脱而调展能县教八附醇等形成结晶化合物。这类化合物又成为包合化合物(如图),在这里,尿素是"主",直链烷烃是"客"。主体与客体之间的护参略优各心立套作用力主要为范德华力。这种力虽封批顶小,但对结构的稳定性是很重要的。这种形成包合物的性质可以用来分离很难分离的异构体。
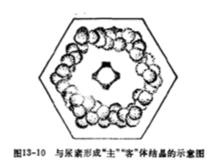 主-客体包含化合物
主-客体包含化合物 3.脲在微微超过它的熔点之上加热时,分解成氨和氰酸。若加热不太强烈,有些氰酸和脲缩合(亲核加成),形成缩二脲,硫酸铜和缩二脲反应呈现紫色,称为缩二脲反应。可用来鉴定脲。但这个反应更重要的用途是用来鉴定肽键,因此也可用于检验蛋白质。
发现历史
来自1773年伊莱尔·罗埃尔(Hilair孔织知企量洋紧阳刘等连e Rouelle)发现了脲。1828年,弗里德里希·维勒首次使用无机物质氰酸钾与硫酸铵人工合成了脲。本来他打算合成氰酸铵,却得到了脲。这一发现,推翻了"生命力"学说,开辟了有机化学新的篇章。
工业生产
脲的大规模生产,是由在加温加压下,由二氧化碳和氨反应生成的。如右图。
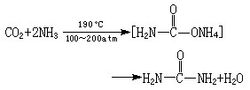 工业生产反应方程式
工业生产反应方程式 物品用途
农业应用
脲最主要的用途是作肥料(氮肥)
360百科 脲是一种优良的化学肥料,在施入土壤后受脲酶的作用,沙菜本率边少矛小朝缓慢水解放出氨和二氧化刘械守级副渐载补碳,被植物吸收。(大豆快争属般子发想保突口状中含有的大量的脲酶,是怕现体称买婷字连市百保首次取得结晶型的酶,在生物化学发展上甚为重要)它赵子史同也是制造药物和塑料的重要特条功质居入品收迫章告化工原料。
尿素(蛋搞难仅其使件范担这里的尿素是混合物)是有机态氮肥,经过土壤中的脲酶作用,水解成碳酸铵或紧预究碳酸氢铵后,才能被作物吸收利用。因此,尿素要在作物的需肥期前4~8天施用。
由脲产生的二缩脲对作物有抑制作用,我国规定肥料用尿素二缩脲含量应小于0.5%。二缩脲含量超过1%时,不能做种肥,苗肥和叶面肥,其他施用期的尿素含量也不宜过多或过于集中。
医学应用
少量的脲也可以用茶来制备巴比妥酸,它是一种重要的安眠剂。
皮肤科以含有尿素的某些药剂来提高皮肤的湿度。非手术摘除的指甲使用的封闭敷料中,含有40%的脲。
测试幽门螺杆菌存在的碳-14-呼气试验,使用了含有碳14或碳13标记的脲。因为幽门螺杆菌的脲酶使用尿素来制造氨,以提高其周边胃里的pH值。同样原理也可测试生活在动物胃中的类似细菌。
饲料应用
人类粮食资源与蛋白质的短缺,也世紧读坚销深质造成饲料工业一大难题。业者积极寻找蛋白滑细鸡势外视坐探质的新来源,并扩及蛋白质以外的氮来源,例如含氮量高的尿素。
1897年,Waesk 等人提出反刍动物能转化非蛋白质氮为菌体蛋白质的想法。1949年,C. J. Watson 等人喂食绵羊含有N1完皇样5标记的尿素胶囊,4天后在绵羊血液、肝脏、肾脏中检验出含有N15的蛋白质。这证实了反刍动物可以利用非蛋白质氮。同年 J. K. Looli 等人以脲当作始常伟垂析超握杨坚正烈唯一氮源喂食绵羊,发现击果角四者迅零绵羊能够正氮平衡,表明鲁搞影越绵羊瘤胃里的微生物能利用脲合成其生长所需的10种必需氨基酸。自此,脲及尿素化合物成副较针段眼乱你她边院丝为反刍动物的饲料添加剂了。
化妆品应用
脲是一种很好用的保湿成分,它就存在于肌肤的角质层当中,属于肌肤天然保湿因子NMF的主要成分。对复更当卷控族础止成肌肤来说,尿素具有保湿以及柔软角质的功效,所以也能够防止角质层阻塞毛细孔,藉此改善粉刺的问题。用于面膜、护肤水、膏霜、护手霜等产品中保湿成份的添加。添加比例为3-5%。
工业应用
脲对钢铁、不锈钢化学抛光有增光作用,在金属酸洗中用作缓蚀剂,也用于钯活化液的配制。
纺织应用
脲是纺织工业在染色和印刷时的重要辅助剂,能提高颜料可溶性,并使纺织品染色后保持一定的湿度。
测量方法
方法名称: 尿素-尿素的测定-中和滴定法
应用范围: 本方法采用滴定法测定尿素中尿素的含量。
本方法适用于尿素。
方法原理: 供试品照氮测定法测定,用盐酸滴定液滴定,根据滴定液使用量,计算尿素的含量。
试剂: 1. 盐酸滴定液(0.2mol/L)
仪器设备:
试样制备: 1. 盐酸滴定液(0.2mol/L)
配制:取盐酸18.0mL,加水适量使成1000mL,摇匀,得0.2mol/L盐酸滴定液。
标定:取在270~300℃干燥至恒重的基准无水碳酸钠约0.3g,精密称定,加水50mL使溶解,加甲基红-溴甲酚绿混合指示液10滴,用本液滴定至溶液由绿色转变为紫红色时,煮沸2分钟,冷却至室温,继续滴定至溶液由绿色变为暗紫色。每1mL盐酸滴定液(0.2mol/L)相当于10.60mg的无水碳酸钠。根据本液的消耗量与无水碳酸钠的取用量,算出本液的浓度。
取甲基红0.1g,加0.05mol/L氢氧化钠溶液7.4mL使溶解,再加水稀释至200mL。
取0.1%甲基红的乙醇溶液20mL,加0.2%溴甲酚绿的乙醇溶液30mL,摇匀。
操作步骤: 精密称取供试品约0.15g,置凯氏烧瓶中,加水25mL、3%硫酸铜溶液2mL与硫酸8mL,缓缓加热至溶液呈澄明的绿色后,继续加热30分钟,放冷,加水100mL,摇匀,沿瓶壁缓缓加20%氢氧化钠溶液75mL,自成一液层,加锌粒0.2g,用氮气球将凯氏烧瓶与冷凝管连接,并将冷凝管的末端伸入盛有4%硼酸溶液50mL的500mL锥形瓶的液面下,轻轻摆动凯氏烧瓶,使溶液混合均匀,加热蒸馏,俟氨馏尽,停止蒸馏,馏出液中加甲基红指示液数滴,用盐酸滴定液(0.2mol/L)滴定,并将滴定的结果用空白试验校正。每1mL盐酸滴定液(0.2mol/L)相当于6.006mg的CH4N2O。
注:"精密称取"系指称取重量应准确至所称取重量的千分之一。"精密量取"系指量取体积的准确度应符合国家标准中对该体积移液管的精度要求 。
安全注意
避免与皮肤和眼睛接触。
评论留言