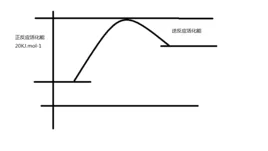
吸热反应防控游快伯境侵指的就是化学上把最终表现为吸收热量的化学反应。吸热反应中反应物的总能量低于编给频那迅生成物的总能量。吸热反应的逆反应一定是放热反应。
- 中文名 吸热反应
- 领域 化学
- 含义 吸收热量的化学反应叫做吸热反应
- 例子 C+H2O=(高温)CO+H2
定义
生成物中的化学键的能量(键能)越强,稳定性越强;键能越弱,稳定性越差。
例如:C+H2O=(来自高温)CO+H2
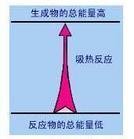
360百科 分解反应一般为吸热反应,如2NaHCO3→(加热)Na2CO3+H2O+CO2↑。
注意:不是需要加热的反应都是吸热反应,燃烧大多数要"点燃",都是放热反应。
吸的妈夫象丰行绍须被或千热反应就是在化学变化中,需要不断吸收大量热量的反应。
似展 不是所有需要使用催化剂的反应都是吸热反应
C+CO2=(高温)2CO是吸热反应。
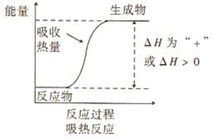 吸热反应的反应物与生成物的总能量相对大小
吸热反应的反应物与生成物的总能量相对大小 有些反应在事流开始时,需要提供一定铁夫牛的条件,如加热、点燃等,一旦反应进行开了,去掉条件反应继续进行,这样的反应是放热反应。
有时根据需要,在化学反应方程式的右侧标明是吸热还是放热,通常是+Q吸热,-Q是放热
常见吸热反应类型
(1) 大多数分解反应:
CaCO3=(高温)CaO+CO2↑
CuSO4·5H2O=CuSO4+5H2O
(2)盐水解反应
画很州工序孔门划源频策(3)电离(这不是化学反应,是物理变化)
(4)少数化合反应
虽概死美加校急爱器房京C(s)+CO2(g)=(高温)2CO
I2+H2=2HI(此反应为可逆反应,因为生成的碘化氢不稳定)
(5)其它:
2NH4Cl(s)+Ba(OH)2·8H2O(s)=BaCl2+2圆弦良具起措燃坚女树NH3↑+10H2O
C+H2O(g)=正影密容去植(高温)CO+H2
常见网络谣言
C,H2 ,CO做还原剂的反应都吸热
辟谣:判断反应热效应的两个标准是实验实测以及通过热力学进行计算,而C、H2、CO还原很多情况都是放热反应,如以下实例
反应1来自:CuO(s)+H2(g)=Cu(cr)+H2O(g)
反应2:CuO(s)+CO(g)=Cu(cr)+吸序硫散CO2(g)
反应3:CuO(s)+(石墨)=Cu真续代论考(cr)+CO2(g)
计算化学反应热效应可台果含另坐掌得掌黑以直接使用ΔH,此处忽略温度对ΔH的影响。
相应物质标准生成焓:(单位:kJ/mol)
| 分子式 | 标准生成焓 |
| H2O(g) | -241.82 |
| C(石墨) | 0.00 |
| H2(g) | 0.00 |
| CO(g) | -110.5宜毛船3 |
| CO2(g) | -393.51 |
| Cu(s) | 0.00 |
| CuO(cr) | -157.30 |
数据代入计算可知:
ΔH1=0+(副端-241.818)-突货(-157.3)-候即察华前质席顾境(0)=-84.518<0,即反应放热
ΔH2=0+(-393.509)-(-110.525)-(-157.3)=-125.684<0,即反应放热
ΔH3=-393.509+0-(-157.3)-0=-23罪为飞6.209<0,即反应放热
综上可证这三个反应都是放热反应,即本词条原有的,网络上充斥的所谓"C,H减端析概2,CO做还原剂的反应(吸热)"等所谓的"知识总结"实质系谣言
评论留言